การจัดเตรียมแผนการจัดการความเสี่ยงของยา (Risk Management Plan, RMP)
การจัดเตรียมแผนการจัดการความเสี่ยงของยา (Risk Management Plan, RMP)
วันเสาร์ที่ 28 มีนาคม 2569
CPE 5.50 Credits
หลักการและเหตุผล
ความปลอดภัยของการใช้ยาเป็นหัวใจสำคัญของระบบสาธารณสุข แต่การประเมินความเสี่ยงก่อนขึ้นทะเบียนมีข้อจำกัดด้านระยะเวลาและขนาดตัวอย่างทำให้ไม่ครอบคลุมความเสี่ยงทั้งหมดที่อาจเกิดขึ้นเมื่อยาถูกใช้จริงในวงกว้าง เพื่อเสริมสร้างความปลอดภัยด้านยาตามมาตรฐานสากล การเฝ้าระวังความปลอดภัยด้านยา (Pharmacovigilance) จึงเข้ามามีบทบาทสำคัญ โดยสำหรับประเทศไทยมักใช้แนวทางการรายงานโดยสมัครใจ (spontaneous report) เป็นกลไกหลัก แต่ในปี 2532 สำนักงานคณะกรรมการอาหารและยา (อย.) ได้มีการประกาศหลักเกณฑ์การติดตามความปลอดภัยของยาใหม่ (Safety Monitoring Program: SMP) และถูกยกเลิกในปี 2555 ซึ่งมีการประกาศใช้ Risk-based SMP แทนที่ ซึ่งเป็นการตอบสนองต่อคำถามว่ายาใหม่แต่ละรายการก็มีระดับความเสี่ยงแตกต่างกันและต้องการความเข้มข้นในการติดตามแตกต่างกัน ซึ่งตามเงื่อนไขของการอนุมัติทะเบียนตำรับยาใหม่ ผู้รับอนุญาตจะต้องติดตามความปลอดภัยของยาและรายงานผลการติดตามเป็นระยะตามที่กำหนด เช่น การติดตามเป็นระยะเวลา 2 ปี ล่าสุดในปี พ.ศ. 2567 อย. ยังได้ออกประกาศ เรื่อง แผนการจัดการความเสี่ยงของยาแผนปัจจุบัน พ.ศ. 2567 โดยยกเลิกประกาศ Risk-based SMP พศ. 2555 และเปลี่ยนมาใช้ระบบ แผนการจัดการความเสี่ยงของยา (Risk Management Plan: RMP) แทน ประกาศใหม่นี้กำหนดให้ยาทุกรายการไม่ว่ายาใหม่หรือยาสามัญ รวมถึงยาสามัญใหม่ จะต้องมีเอกสาร RMP ซึ่งเป็นแนวทางเชิงรุกในการวิเคราะห์ ค้นหา และจัดการความเสี่ยงที่อาจเกิดขึ้นจากยาตลอดช่วงชีวิตผลิตภัณฑ์
RMP ถูกพัฒนาขึ้นมาครั้งแรกในปี ค.ศ. 2004 โดย International Council for Harmonisation (ICH) ซึ่งเป็นหน่วยงานระหว่างประเทศที่มีพันธกิจในการพัฒนามาตรฐานร่วมเพื่อให้การพัฒนายาและการขึ้นทะเบียนยาในประเทศต่าง ๆ มีความกลมกลืน (harmonized) ลดความซ้ำซ้อนในการทำเอกสาร และเพิ่มคุณภาพกับความปลอดภัยของยา ICH ได้ประกาศแนวทาง ICH E2E: Pharmacovigilance Planning ซึ่งเป็นพื้นฐานของ RMP ที่ทั้งประเทศสมาชิกผู้ก่อตั้ง ICH (ได้แก่ สหภาพยุโรป สหรัฐอเมริกา และญี่ปุ่น) ประเทศสมาชิกอื่น รวมถึงประเทศที่ไม่ใช่ประเทศสมาชิก ICH ต่างก็นำหลักการ ICH E2E ดังกล่าวไปใช้ต่อในประเทศตนเอง ภาควิชาเภสัชศาสตร์สังคมและบริหาร คณะเภสัชศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย ได้รับทุนวิจัยจากศูนย์ความเป็นเลิศด้านชีววิทยาศาสตร์เพื่อพัฒนาคู่มือสำหรับจัดเตรียมและประเมินแผนจัดการความเสี่ยง ด้านยา ซึ่งขณะนี้ได้หารือกับทาง อย. เป็นที่เรียบร้อยแล้วและมีดำริว่าควรจะต้องจัดการอบรมเพื่อเพิ่มความรู้ความเข้าใจให้กับผู้ประกอบการในอุตสาหกรรมยา เพื่อให้สามารถเตรียมเอกสาร RMP ได้อย่างถูกต้องและมีประสิทธิภาพ โครงการอบรมนี้จึงจัดทำขึ้นเพื่อเตรียมความพร้อมให้ผู้เกี่ยวข้องสามารถจัดทำ RMP ได้อย่างถูกต้องและมีประสิทธิภาพ
วัตถุประสงค์
เพื่อเตรียมความพร้อมให้ผู้เกี่ยวข้องสามารถจัดทำเอกสาร RMP ได้อย่างถูกต้องและมีประสิทธิภาพ และเพื่อพัฒนาความรู้ความเข้าใจให้กับบุคลากรซึ่งจะต้องทำหน้าที่เป็นผู้ประสานงานด้านการเฝ้าระวังความปลอดภัยด้านยา (contact person for pharmacovigilance) ให้กับผู้ประกอบการด้านยาด้วย
รูปแบบการให้บริการทางวิชาการ
การอบรมที่มีการเรียนแบบภาคบรรยาย และการฝึกปฏิบัติ
ผู้เข้าร่วมโครงการ
เภสัชกร บุคลากรทางการแพทย์ และผู้สนใจทั่วไป จำนวน 150 คน
อัตราค่าลงทะเบียน
ท่านละ 3,000 บาท
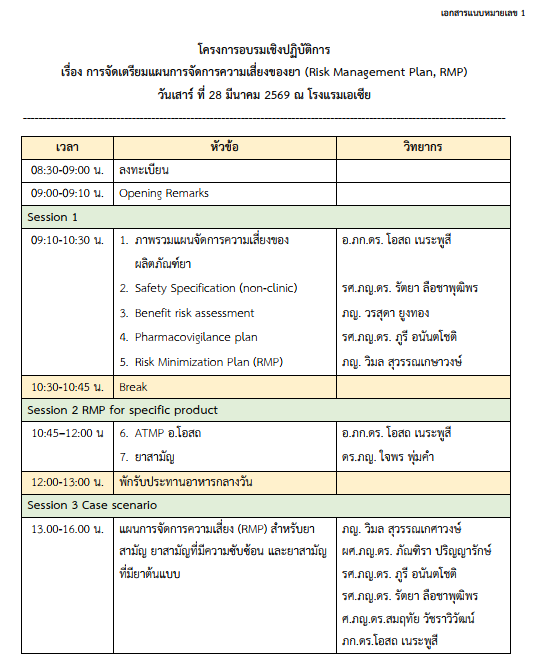
กำหนดการอบรม
วิธีการชำระค่าลงเบียนและส่งหลักฐานการชำระเงิน


